CCS, CCUS EP8 – Dissolution Trapping – CCS ตอนที่ 8 ชวนคุยเรื่องโซดาใต้ดินกับกลไกการคงค้างแบบละลาย (Dissolution Trapping)
สวัสดีครับทุกท่าน หลังจากที่ตอนที่แล้วผมได้อธิบายว่าไอเจ้า CO2 มันไปติดแหง็กอยู่ในรูพรุน (Residual Trapping) ได้ยังไงแล้วเนี่ย…. แต่มันยังไม่สุดครับ! มันเหมือนเราจับขังมันไว้ในคุก แต่ถ้าวันดีคืนดีคุกแตกมันก็อาจจะหนีกลับขึ้นมาได้ใช่ไหมล่ะ?
CCS CCUS EP7 residual trapping – capillary trapping
CCS, CCUS EP8 – Dissolution Trapping
คราวนี้เราจะมาพูดถึงวิธีที่ เด็ดขาด กว่านั้น! นั่นคือการ “แปลงสภาพ” เจ้า CO2 ให้มันกลายเป็นมิตรและเป็นอันหนึ่งอันเดียวกับเจ้าบ้านใต้ดินไปเลย! กลไกนี้แหละครับที่เรียกว่า กลไกการคงค้างแบบการละลาย (Dissolution Trapping)
กลไกการคงค้างแบบการละลาย (Dissolution trapping)
– ไอเจ้ากลไกการคงค้างแบบการละลายเนี่ยแนวคิดนี้มันมาก่อนกาลกว่า CCS แล้วแหละครับ 5555 ถ้าให้ผมเดาเราๆ ท่านๆ ก็น่าจะคุ้นเคยกันดีครับผม ก็โซดาในวงเหล้านั่นแหละ 555 หลักการแบบเดียวกันเป๊ะเลยครับกับพวกบริษัทที่ผลิตโซดา หรือน้ำอัดลม คือเราพยายามที่จะเอา CO2 ละลายเข้าไปอยู่รวมกับน้ำให้ได้น้ำอัดลมครับ
แต่ถ้าหากใครที่เคยกินเยอะๆ จนปวดท้องหรือไปพบคุณหมอ คุณหมอก็จะบอกว่า น้ำอัดลมเนี่ยมันมีกรดมันกรดนะ กรดนั้นคือกรดอะไร? เกี่ยวข้องยังไงกับงาน CCS เรามาหาคำตอบกันด้านล่างครับ
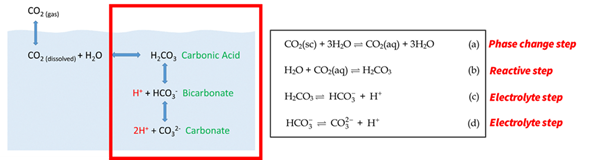
รูปที่ 1 เครดิตรูปภาพด้านซ้าย: 5.5 Dissolved Gases: Carbon Dioxide, pH, and Ocean Acidification – Introduction to Oceanography ฝั่งขวาผมเขียนเอง
รูปภาพด้านบนที่คุณเห็นนั้นคือกลไกการละลายของก๊าซ CO2 มาอยู่ในน้ำครับโดยมันจะเกิดปฏิกิริยาเคมีหลักๆ เป็นแปลงร่างเป็นกรดคาร์บอนิก (Carbonic Acid) กรดคาร์บอนิก H2CO3 (ตอนกินน้ำอัดลมแล้วมันไปกัดกระเพาะนั้นแหละ)
แต่เรื่องมันไม่ได้จบแค่นั้น! พอผ่านคืนวันเนิ่นนานไป ไอเจ้ากรดคาร์บอนิกนี่มันจะเริ่ม แตกตัวออก ตามอุณหภูมิและความดัน กลายเป็นสารประกอบจำพวก ไบคาร์บอเนต (Bicarbonate) และ คาร์บอเนต (Carbonate) ไอ้พวกสารประกอบพวกนี้แหละคือ พระเอกตัวจริง ที่เตรียมจะไปสร้างแร่หินในสเต็ปถัดไปครับ
-------------------------------------------------------
ไม่พลาด ข่าวสาร บทความ ความรู้ ประกาศตำแหน่งงานว่าง และ อื่นๆ
กรอก ชื่อ และ อีเมล์ ในแบบฟอร์มข้างล่าง จะมีอีเมล์กลับมาให้ "ยืนยัน" นะครับ การสมัครจึงจะสมบูรณ์ ... อ้อ ... อย่าลืมดูใน junk, trash, spam box นะครับ บางทีระบบมันเอาอีเมล์ตอบกลับไปไว้ที่นั่น
ฟังดูง่ายใช่ไหมครับ? 555 แต่โลกความจริงมันไม่ง่ายอย่างนั้น! บอกเลยว่าตอนนี้เรากำลัง ข้ามศาสตร์ จากวิศวกรรมปิโตรเลียมไปหาวิศวกรรมเคมีเต็มตัวแล้วครับ!
เพราะการอธิบายเรื่องนี้มันต้องเข้าใจปรากฏการณ์ การถ่ายโอนมวล (Mass transfer) ซึ่งน้องๆ วิศวะเคมีที่เรียนเรื่องนี้ก็จะ “ร้องกันระงม” เพราะมันยากครับ! 555 แต่ไม่ต้องห่วง! ผมจะอธิบายแบบง่ายโคตรๆ ให้ดูครับ!
หลักการแรงขับ (Driving Force) แบบง่ายโคตรๆ! จำได้ไหมว่าตอนเราอัด CO2 เข้าไปนั้น เราอัดเข้าไปในรูปของ ของไหลวิกฤตยิ่งยวด (Supercritical Fluid: sc) ซึ่งโดยหลักการทั่วไปของการละลายและการแพร่ (dissolution and dispersion) เนี่ย มันจะเริ่มจาก ความเข้มข้นสูงไปหาความเข้มข้นต่ำเสมอ
ไอ้เจ้าความเข้มข้นสูงนี่แหละครับที่เราเรียกมันว่า “แรงขับ” (Driving Force) ถ้าความเข้มข้นต้นทางกับปลายทางมันเท่ากันเมื่อไหร่… มันจะเข้าหาสิ่งที่เรียกว่าจุดสมดุลและมันจะหยุดละลายทันที
หลักการนี้ใช้ได้กับทุกอย่างบนโลกครับ! เหมือนน้ำไหลในท่อเด๊ะๆ: ถ้าเราอยากให้น้ำไหลจากซ้ายไปขวา แรงดันฝั่งซ้ายก็ต้องมากกว่าฝั่งขวาถูกไหม? ถ้าแรงดันเท่ากัน น้ำก็ไม่ไหล! ง่ายๆ แบบนี้เลยจริง ฮ่าๆ 55
ผมขออนุญาตนำเสนอการทดลองด้านล่างให้เห็นภาพนะครับ

รูปที่ 2 แคปมาจาก VDO เครดิต: Rate of Dissolving, Hot and Cold Water lab Demonstration
รูปที่ 2.1: เริ่มแรกหยดลงไปยังเป็นน้ำเปล่าใสๆ ครับ
รูปที่ 2.2: มีการหยดน้ำสีฟ้าความเข้มข้นสูง (สีฟ้าเข้ม) ลงไป ความเข้มข้นจะเริ่มกระจายตัวออกครับ
รูปที่ 2.3: น้ำสีฟ้ากระจายตัว ลงไปในน้ำเปล่า
- ถ้าเราอยากทำให้มันผสมเข้ากันไวๆ? ก็เอาช้อนมาคนให้มันแพร่ได้ไวยิ่งขึ้นไงล่ะครับ!
- แต่ถ้าเราทิ้งไว้นานพอโดยที่ไม่ไปยุ่งกับมัน สีฟ้าก็จะกลายเป็นสีเดียวกันทั้งแก้วครับ นั่นแปลว่าความเข้มข้นมันเท่ากันหมดแล้ว… มันก็หยุดละลายแล้วครับ!
ฟังดูเป็นสามัญสำนึก แต่ในโลกวิศวกรรมเคมีนั้นมี “กฎเหล็ก” ที่อธิบายเรื่องนี้แบบเป๊ะๆ ซึ่งก็คือ กฎของฟิก (Fick’s Law) นั่นเองครับ
หน้าตาของสมการที่ใช้อธิบายกฎของฟิคหน้าตาจะเป็นดังนี้ครับ
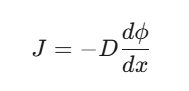
ตัว J: คือ อัตราการแพร่ (Flux) ของ CO2 ครับ (พูดง่ายๆ คือ ความเร็ว ที่ CO2 วิ่งเข้าสู่สารละลาย)
ตัว D: คือ สัมประสิทธิ์การแพร่ (Diffusion Coefficient) เป็นค่าที่บอกว่า CO2 มันวิ่งได้คล่องแค่ไหนในตัวกลางนั้น ๆ (น้ำเกลือ)
d(phi)/dx: คือ ความชันของความเข้มข้น ครับ (phi คือความเข้มข้น และ x คือระยะทาง) นี่แหละครับคือ “แรงขับ” (Driving Force) ตัวจริง!
เครื่องหมายลบ (-): ใส่ไว้เพื่อบอกว่าการแพร่จะเกิดจากที่ที่มีความเข้มข้น สูง ไปหาความเข้มข้น ต่ำ เสมอครับ
กฎของฟิกมันว่าไว้ว่า “อัตราการแพร่ (Flux)” ของสารเคมี (ในที่นี้คือ CO2) เนี่ย มันจะ แปรผันตรงกับ “ความเข้มข้น”
พูดง่ายๆ คือ ถ้าความเข้มข้นของ CO2 ในรูป (sc) ใกล้กับชั้นหินปิดกั้น (มี CO2 เกือบจะล้วนๆ) กับ CO2 ที่ละลายในน้ำ (ด้านล่าง) มัน “ต่างกันมาก” อัตราการละลายก็จะ “เร็วมาก”
กลับกันครับ ถ้าหาก CO2 ที่ละลายอยู่ในน้ำมีความเข้มข้นใกล้เคียงกันกับ CO2 ที่ยังไม่ละลายลงมา อัตราการละลายก็จะต่ำมากๆ เช่นกันครับ
เชื่อไหมครับว่ามนุษย์เรามีสัญชาตญาณเรื่องการละลายและการแพร่กันอยู่แล้ว แม้ว่าคุณจะไม่ได้สนใจทฤษฎีมันเลยก็ตาม…
ลองนึกภาพตอนคุณสั่ง ก๋วยเตี๋ยวแห้ง สิครับ..
- คุณปรุงก๋วยเตี๋ยวใส่ น้ำปลา น้ำตาล พริกป่น ลงไป (นี่คือการสร้าง “ความเข้มข้นสูง”)
- คุณก็ต้อง คนๆ คลุกเคล้า ใช่ไหมครับ?
การที่คุณ “คน” นั่นแหละครับคือการ “เร่ง” ให้เครื่องปรุงมันละลายและกระจายตัว (แพร่) ในชามได้ดีขึ้น ซึ่งในทางเทคนิคก็คือการเร่งให้การแพร่ได้ไวยิ่งขึ้นครับ!
แต่ถ้าหากคุณใจเย็น รอมันอีกสักนิด ให้เวลามันกระจายตัวรับรองอร่อยเหมือนเดิมครับ 555 ล้อเล่น ก๋วยเตี๋ยวรสชาติจะเด็ดขึ้นแน่นอนครับ เพราะเครื่องปรุงมันได้ละลายและแพร่ซึมซับเข้าเส้นและเนื้อได้ทั่วถึงแล้ว!
นี่แหละครับคือ “แรงขับ” (Driving Force) ตัวจริง! ในงาน CCS เราก็หวังให้มีแรงขับสูงๆ ในช่วงแรก เพื่อให้ CO2 มันละลายตัวลงน้ำให้เร็วที่สุดเท่าที่จะทำได้ครับ!
ประเด็นหลักคือมันเอาไปใช้ยังไงกับ CO2 ในเรื่อง CCS หละ? แน่นอนครับว่าการละลายของ CO2 ลงไปในน้ำที่อยู่ในช่องว่างของพรุนก็จะเป็นในลักษณะคล้ายๆ กันแต่จะมีการแตกขั้นตอนออกมาดังนี้ครับ
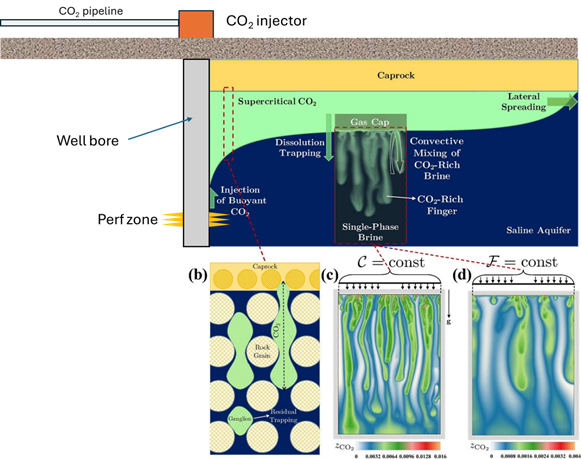
รูปที่ 3 เครดิตรูปภาพต้นฉบับ (ที่เหลือผมต่อเติมมา55): Overview of structural, residual, and dissolution trapping mechanisms… | Download Scientific Diagram
ในช่วงแรก CO2 จะค่อยๆลอยขึ้นด้านบนไปสะสมตัวอยู่กับชั้นหินปิดกั้น (cap rock) ซึ่งยังคงดำรงสถานะ sc อยู่จากนั้น CO2 ที่อยู่ใกล้ๆกับหลุมอัดของเราบางส่วนจะโดน residual trapping ตามรูป b ที่ขยายออกมาครับ
กลุ่มก้อน CO2 (gas cap) ที่ขึ้นไปกองกันที่ชั้นหินปิดกั้นจะเริ่มแยกชั้นกับน้ำในแหล่งกักเก็บอย่างชัดเจน ซึ่งไอเจ้า CO2 ตรงขอบรอยต่อระหว่างน้ำกับกลุ่มก๊าซ (gas cap) จะเริ่มเกิดการเปลี่ยนสถานะจาก sc ไปเป็นของเหลวหรือสารสะลาย (aq) ครับ ซึ่งในขั้นแรกผมจะเรียกว่า phase change step การเปลี่ยนแปลงจะเป็นไปตามสมการเคมีสีแดงในรูปที่ 1 ซ้ายมือครับ
จากนั้น CO2 ที่อยู่ในรูปสารละลายเนี่ยครับ ตัวสารละลายมันค่อยๆหนักขึ้น (ความหนาแน่นมากขึ้น) ทำให้มันจมลงไปในน้ำดังด้านล่างตามรูปขยาย c และ d เป็นทางแนวยาวของความเข้มข้นของ CO2 ซึ่งในทางเทคนิคเราจะเรียกว่าปรากฎการณ์ Fingering (เพราะมันดูคล้ายนิ้วมือนั้นแหละครับ) ไอเจ้าเส้นแถบยาวๆของความเข้มข้นเนี่ย CO2 เนี่ย จะเริ่มทำปฏิกิริยากับน้ำเกลือกลายเป็นกรดคาร์บอนิกครับ (H2CO3) ซึ่งผมเรียกว่า reactive Step เนื่องจากมันเกิดปฏิกิริยาเคมีนั้นเอง
จากนั้นเมื่อเวลาผ่านไปเนิ่นนานมากพอจะเกิดเป็นปฏิกิริยาการแตกตัวของกรดในน้ำ (Electrolyte) เป็นไบคาร์บอเนต (HCO3–) แล้วแตกตัวต่อออกมาเป็นสารประกอบคาร์บอเนต (CO32-) ไอเจ้าการแตกตัวเนี่ย เป็นการเตรียมความพร้อมสำหรับกลไกสุดท้ายที่ถาวรที่สุด… ซึ่งเราเรียกว่า mineralization ครับ
ข้อจำกัดครับ..
ทั้งนี้ทั้งนั้นหากใครกลับไปดูรูป trapping mechanism ในตอนที่แล้ว จะเห็นได้ว่ากลไกนี้ใช้เวลานานมากๆ เลยใช่ไหมครับ ตั้งแต่หลัก 10 ปีถึงหมื่นปีเลยทีเดียว ซึ่งตัวที่บ่งชี้ว่าจะละลายช้าหรือเร็ว เราจะเรียกว่าความสามารถในการละลายครับ (solubility) ซึ่งมันขึ้นอยู่กับหลายปัจจัยมากๆ เช่น อุณหภูมิ และ ความดันของแหล่ง, ค่าความเค็มของน้ำในแหล่งที่เราจะกักเก็บ, แร่ธาตุองค์ประกอบที่อยู่ในแหล่งกักเก็บเป็นต้นครับ
ซึ่งปัจจัยเหล่านี้แหละ น้องๆ วิศวกรรมเคมีจะตอบเราได้ครับ 555 ว่าความสารถในการละลายมันจะใช้เวลามากน้อยแค่ไหน
ช่วงชี้ช่องรวย (อีกแล้ว!) 555 ถ้าคุณจำวิชาเคมีสมัยมัธยมได้… เราสามารถทำให้ปฏิกิริยาเคมีมันเกิดขึ้น เร็วขึ้น ได้ ถ้าเรามี ตัวเร่งปฏิกิริยา ใช่ไหมครับ??
นั่นแหละครับ! ถ้าใครในอนาคตอ่านแล้วเกิดคิดขึ้นมาได้ว่า จะหาวิธีเร่งให้มันละลายไวขึ้นเป็นบ้าเป็นหลังได้อย่างไร… อย่าลืมมาเรียกผมกับลุงนกด้วยนะครับ! 555 ถ้าเราย่นเวลาได้เร็วขึ้นเป็นหลัก 100 ปี… บอกเลยว่าบริษัทน้ำมันก็จะมารุมซื้อกันแล้วครับ! 5555
ตอนนี้เนื้อหาอาจจะหนักหรือยาวไปบ้าง แต่ก็ขอบคุณที่ติดตามอ่านกันมาจนจบนะครับ!
ตอนหน้าผมจะพาไปรู้จักกับการเกิดแร่สำหรับ mineral trapping ครับผม แล้วจะมา บอกถึงข้อเสียของเทคโนโลยีนี้กันครับ
ขอแอบสปอยล์นิดนึงว่า CCS ไม่ใช่ทุกประเทศที่ทำได้นะครับ อิอิ
Nautilus (Tuna) – nattirut.ys@gmail.com
Special thanks to PEwoF team
CCS, CCUS EP 9 Mineralization Trapping
ถ้าจะซื้อของออนไลน์จาก 2 เจ้านี้อยู่แล้ว คลิ๊กลิงค์ หรือ โลโก้ ข้างล่างนี้เลยครับ ผมจะได้ค่าคอมฯเล็กๆน้อยๆสมทบทุนจ่ายค่าเช่า host server ขอบคุณครับ
(ไม่ต้องกังวลนะครับ ไม่ใช่ลิงค์ดูดเงินแน่ๆ)
 https://raka.is/r/qlzXR https://raka.is/r/qlzXR |
 https://raka.is/r/gP7GV https://raka.is/r/gP7GV |


